Therapie von Kinderrheuma
Das Team der Klinik für Kinder- und Jugendrheumatologie legt großen Wert auf eine interdisziplinäre und ganzheitliche Therapie, damit Kinder und Jugendliche mit Gelenkentzündungen und –schmerzen schnell wieder in ihren schulischen und sportlichen Alltag zurückfinden.

Viele Bausteine für eine ganzheitliche Therapie
Wichtige Therapiebestandteile neben der medikamentösen Therapie sind physikalische Maßnahmen wie z. B. Kältebehandlung, Physiotherapie, Ergotherapie sowie auch die Elternanleitung zur Fortführung der Übungsbehandlung zu Hause. Kindgerechte orthopädische Hilfsmittel werden in der hauseigenen Orthopädischen Werkstatt oder in der Abteilung für Ergotherapie individuell hergestellt. Sie korrigieren rheumatisch bedingte Wachstumsstörungen und Fehlentwicklungen.
Die antirheumatische Therapie richtet sich nach dem individuellen Krankheitsverlauf unter Berücksichtigung der altersabhängigen Besonderheiten. Neben der modernen medikamentösen Therapie (z.B. mit Immunsupressiva, Biologika oder JAK-Hemmern) führen die Ärztinnen und Ärzte gezielte Gelenkpunktionen (auch unter Ultraschallführung) bei Kindern und Jugendlichen durch.

Psychosoziale Betreuung
Ein psychosoziales Team, bestehend aus Expertinnen und Experten aus Medizin, Kinderkrankenpflege, Psychologie, Erzieherinnen, Sozialarbeiterinnen sowie Lehrerinnen und Lehrern der Schule im St. Josef-Stift, unterstützt, fördert und berät die jungen Patientinnen und Patienten sowie deren Eltern umfassend. Kontakte zu Beratungsstellen, Reha-Einrichtungen und Selbsthilfegruppen (z.B. Rheuma-Liga) werden hergestellt.

Selbsthilfe & Klinikschule
Wichtige Ansprechpartner in unserer Klinik sind der Bundesverband Kinderrheuma e.V. mit seinem Familienbüro im St. Josef-Stift. Das Team organisiert Seminare und fördert den Austausch untereinander. Schulpflichtige Kinder und Jugendliche erhalten in der Schule im St. Josef-Stift in den Kernfächern Unterricht, der mit der Heimatschule eng abgestimmt wird.
Medikamente zur Behandlung von Kinderrheuma
Bei den antientzündlich wirksamen Medikamenten unterscheidet man verschiedene Medikamentengruppen, die innerhalb des Entzündungssystems unterschiedliche Angriffspunkte haben. Um Kindern die Wirkweise erklären zu können, werden Tiermodelle für die unterschiedlichen Eigenschaften der Medikamente verwendet.
Nichtsteroidale Antirheumatika (Maus-Medikamente)
Die nichtsteroidalen Antirheumatika (NSAR) sind nicht cortisonhaltige Antirheumatika und kontrollieren den Schmerz und die aktive Gelenkentzündung. Durch Hemmung der Entstehung von Entzündungseiweißen greifen sie auf der Ebene des Gelenks in das Entzündungsgeschehen ein.
Sie wirken innerhalb kurzer Zeit auf die örtliche Entzündung und müssen in der Regel mehrmals täglich gegeben werden.
Wegen ihres schnellen Wirkungseintritts, jedoch wegen einer nur eingeschränkten Bedeutung für den Gesamtverlauf der Erkrankung, bezeichnen wir sie als Maus-Medikamente.
Einige Medikamente stehen auch in Saftform zur Verfügung und können so individuell altersentsprechend dosiert werden.
Als Saft steht z. B. Ibuprofen zur Verfügung, muss jedoch 3 x täglich gegeben werden. Naproxen ist in Saftform nur über die internationale Apotheke erhältlich. Diese Substanz wird in der Kinderrheumatologie gerne eingesetzt, da sie nur 2 x täglich gegeben werden muss. Allerdings muss wegen der möglichen Nebenwirkungen an der Haut auf konsequenten Lichtschutz geachtet werden.
Einige Substanzen liegen auch in einer Verzögerungsform vor und haben daher eine längere Wirksamkeit, z. B. bei Diclofenac gibt es ein Retard-Präparat.
Neuere Entwicklungen dieser Medikamente zielen darauf ab, ein im Entzündungsgewebe entstehendes Eiweiß gezielt zu hemmen. Das Medikament Meloxicam ist dem Naproxen vergleichbar, wirkt deutlich stärker auf diesen Mechanismus und muss nur 1 x täglich gegeben werden.
Die neueren Medikamententwicklungen wurden unter dem Gesichtspunkt einer besseren Verträglichkeit für den Magen- Darmtrakt konzipiert. Sie sind nicht stärker wirksam als die älteren, besser bekannten Medikamente. Man erhofft sich weniger Nebenwirkungen auf den Magen-Darm-Trakt. Diese treten jedoch bei Kindern und Jugendlichen eher selten auf. In der Kinderrheumatologie werden diese Medikamente eher zurückhaltend eingesetzt, z. B. bei Magen-Darm-Unverträglichkeit oder fehlendem Ansprechen auf die gebräuchlichen NSAR. In diesem Fall können Celecoxib oder Rofecoxib eingesetzt werden (ab dem Alter von 16 Jahren zugelassen).
Die früher eingesetzte Acetylsalicylsäure (Aspirin) wird wegen der benötigten hohen Dosierung und der damit verbundenen Nebenwirkungsrisiken nur noch bei sehr speziellen Indikationen zur Rheumabehandlung eingesetzt. Bei den NSAR ist besonders auf Veränderungen der Magen-Darmschleimhaut zu achten. Auch eine Störung der Nierenfunktion, Blutungsneigung und zentral-nervöse Nebenwirkungen wie Kopfschmerzen und Konzentrationsstörungen können auftreten. Unter der Therapie sind daher regelmäßige Kontrollen des Blutes und Urins erforderlich.
Nicht cortisonhaltige Antirheumatika werden bereits zu Beginn der Erkrankung eingesetzt, sobald eine akute Gelenkentzündung gesichert ist. Die Kombination mit Krankengymnastik und physikalischer Therapie (Eisbehandlung der betroffenen Gelenke) ist sinnvoll.
Nach Ansprechen auf andere (Basis-)Medikamente und Abklingen der akuten Entzündung wird eine Dosisreduktion oder Beendigung der Therapie angestrebt.
Basistherapeutika (lang wirksame Antirheumatika – Nilpferd-Medikamente)
Als Basistherapeutika bzw. lang wirksame Antirheumatika werden Medikamente bezeichnet, die die Krankheitsaktivität der chronischen Entzündung auf lange Sicht verändern sollen. Sie führen zu einer Änderung der Reaktionsbereitschaft des Immunsystems, das bei rheumatischen Erkrankungen „überreagiert“ und gegen den eigenen Körper arbeitet. Sie haben die Aufgabe, diese Überreaktion des Immunsystems auf ein normales Maß zu reduzieren. In der Patientenschulung werden diese Medikamente auch als „Nilpferd-Medikamente“ bezeichnet, da sie ähnlich wie das Nilpferd eine große Kraft besitzen, um den Verlauf der rheumatischen Erkrankung zu ändern. Allerdings dauert der Wirkeintritt dieser Medikamente 6 – 12 Wochen, so dass ihre Wirkung erst im Langzeitverlauf beurteilt werden kann.
Methotrexat (Basistherapie)
Methotrexat ist Mittel der Wahl bei chronisch entzündlichen Gelenkerkrankungen im Kindes- und Jugendalter. Methotrexat hat einen komplexen Wirkmechanismus auf die Entzündungsaktivität in der Zelle, unter anderem auch als Gegenspieler der Folsäure. Daneben gibt es auch Folsäure-unabhängige entzündungshemmende Wirkungen.
Die Wirksamkeit ist in kontrollierten Studien sehr gut belegt. In der Wirkdosis von 10 – 15 mg/m² Körperoberfläche sprechen etwa 60 – 70 % der Patienten gut auf dieses Medikament an. Es bestehen mittlerweile mehr als 30 Jahre Erfahrung mit diesem Medikament in der Kinder- und Jugendrheumatologie. Es wird in den Therapieleitlinien zur juvenilen idiopathischen Arthritis (JIA) empfohlen und ist zugelassen ab einem Alter von 2 Jahren für Verlaufsformen der JIA mit Befall vieler Gelenke. Es gibt die Möglichkeit der oralen (als Tablette) und der parenteralen Verabreichung (als Spritze oder Pen subcutan, das heißt unter die Haut), die einmal pro Woche erfolgt. In der Langzeitwirkung sind beide Verabreichungsformen wohl gleichwertig. Es kann jedoch ein Unterschied in der Verträglichkeit und Nebenwirkungsrate bestehen. Die Eltern bzw. Kinder lernen den Mechanismus der Injektion (Fertigspritze oder -pen) schnell.
Aufgrund möglicher Symptome des Magen-Darm-Traktes wie Übelkeit und Abneigung bietet sich die Verabreichung abends an, damit diese Nebenwirkung „verschlafen“ wird.
Treten dennoch entsprechende Beschwerden auf, gibt es verschiedene Möglichkeiten der Behandlung. So kann am Tag nach der Methotrexat-Verabreichung Folsäure (5 mg 24h nach MTX) gegeben werden. Auch bestehen gute Erfahrungen mit Akupressurbändern oder einer Aufteilung der Dosis auf zwei verschiedene Tage. Unter Umständen ist sogar eine kinderpsychologische Verhaltenstherapie sinnvoll. Um die Entstehung dieser Nebenwirkungen nicht noch zusätzlich zu verstärken, sollte man sein Kind beobachten, aber nicht nach Nebenwirkungen fragen. Ferner ist die vorübergehende Erhöhung der Transaminasen (Leberwerte) eine häufigere Nebenwirkung. Daher sollten in regelmäßigen Abständen, nach Absprache mit dem Kinderrheumatologen, Laborkontrollen erfolgen, die unter anderem auch die Entzündungsaktivität (Blutsenkungsgeschwindigkeit; CRP), das Blutbild mit roten (Erythrozyten) und weißen Blutkörperchen (Leukozyten), die Blutplättchen (Thrombozyten) und den Blutausstrich (Differenzialblutbild), die Nierenwerte (Kreatinin), die Leberwerte (GOT, GPT) und den Urinstatus umfassen.
Wenige Patientinnen und Patienten klagen über gehäufte bakterielle Infekte, die frühzeitig (antibiotisch) zu behandeln sind, oder über Schleimhautveränderungen im Mund. Unter Methotrexat sollten Impfungen immer kinderrheumatologisch abgeklärt und geplant werden.
Da die Einnahme von MTX ein erhöhtes Risiko für Missbildungen für das ungeborene Kind mit sich bringt, ist auf sichere Verhütungsmaßnahmen (für beide Geschlechter) zu achten. Bei Kinderwunsch sollte es rechtzeitig abgesetzt werden. Auch sollten schwangere Mütter die Substanz nicht verabreichen.
Sulfasalzin (Basistherapie)
Das Präparat Sulfasalazin wirkt auf das Immunsystem des Darmes und wird in der Kinder- und Jugendmedizin bereits seit Jahrzehnten zur Behandlung chronischer Darmentzündungen eingesetzt. Der genaue Wirkmechanismus ist komplex und teilweise unbekannt.
In einer Studie konnte die Wirksamkeit bei JIA auch über einen längeren Zeitraum nachgewiesen werden. Sulfasalazin (Azulfidine RA) wird insbesondere bei einer rheumatischen Erkrankung eingesetzt, bei der der Blutwert HLA-B27 nachweisbar ist. In dieser Untergruppe der JIA (Enthesitis-assoziierte Arthritis; EAA) ist ein relativ gutes Ansprechen nachgewiesen. Sulfasalazin ist zugelassen zur Behandlung der JIA ab 6 Jahren.
Die als „Enthesitis assoziierte Arthritis“ bezeichneten entzündlich rheumatischen Erkrankungen treten häufiger bei Jungen auf. Sie werden gelegentlich auch durch Infektionen angestoßen oder verschlechtert. Diese Gruppe von rheumatischen Erkrankungen zeigt einen sehr unterschiedlichen Langzeitverlauf. Hier muss insbesondere auf eine mögliche Beteiligung der Wirbelsäule geachtet werden. Die Erkrankung kann sich im Verlauf verändern. Daher ist auch auf das Auftreten chronischer Durchfallerkrankungen mit Darmentzündungen oder die Entwicklung einer Schuppenflechte (an Haut, Nägeln, Haaransatz) im Langzeitverlauf zu achten.
Die Dosis wird in den ersten Wochen einschleichend aufgebaut. Vielfältige Nebenwirkungen sind beschrieben, unter anderem Übelkeit, Erbrechen, Durchfälle, Kopfschmerzen, Geschmacksstörungen, Störungen der Leber- und Nierenfunktion, Entzündung der Bauchspeicheldrüse, allergische Hauterscheinungen, Fieber, Funktionsstörung des Knochenmarks, der Abwehreiweiße, der Spermienproduktion. In der Langzeittherapie muss der klinische Verlauf der rheumatischen Erkrankung und die Verträglichkeit regelmäßig überwacht werden. Bestimmte Blutwerte, wie z. B. das Blutbild mit der Anzahl der weißen Blutkörperchen (Leukozyten), Leberwerte, der Funktionswert der Bauchspeicheldrüse (Amylase) und der Niere (Kreatinin) sowie Urinkontrollen sollten als regelmäßige Therapiekontrollen durchgeführt werden.
Leflunomid (Basistherapie)
Leflunomid hemmt die Neuherstellung von bestimmten Eiweißen und hat einen entzündungshemmenden Effekt auf weiße Blutkörperchen (Lymphozyten). Es wurde eine vergleichende Untersuchung mit MTX bei polyartikulärer JIA durchgeführt. Diese erbrachte eine vergleichbare, etwas schwächere Wirksamkeit. Bei Erwachsenen ist diese Substanz eine Alternative bei Unverträglichkeit von MTX. Bisher ist die Substanz für die JIA nicht zugelassen.
An Nebenwirkungen der Therapie ist auf Übelkeit, Durchfälle, Erhöhung der Leberwerte, Veränderungen des Blutbildes, Hautausschläge und Haarausfall zu achten. Bei eingeschränkter Nieren- oder Leberfunktion, Störung des Immunsystems oder eingeschränkter Knochenmarksfunktion darf es nicht gegeben werden. Das Medikament bleibt sehr lange im Körper. Es sollte daher bei geplanter Schwangerschaft nicht angewandt werden. Auf sichere Verhütungsmaßnahmen ist zu achten.
Cortison-Präparate (Tiger-Medikamente)
Kein anderes Medikament wird so kontrovers diskutiert wie Cortison. Es ist biologisch ein körpereigenes Hormon, das von der Nebenniere produziert wird und für das tägliche Leben notwendig ist. Es wird vorwiegend in den frühen Morgenstunden ausgeschüttet und hat unter anderem die Aufgabe, den Körper vom Nachtrhythmus in den Tagrhythmus umzustellen. Als klassisches Stresshormon wird es in Zeiten von Entzündungen und besonderen Anforderungen an den Körper vermehrt ausgeschüttet. Jedoch reicht auch diese vermehrte Ausschüttung nicht, um eine Entzündung durch körpereigene Mechanismen ausreichend zu behandeln. Daher werden Cortisonpräparate wegen ihrer starken antientzündlichen Wirkung therapeutisch eingesetzt. Cortison ist aus modernen Therapiekonzepten nicht mehr wegzudenken.
In der Klinik für Kinder- und Jugendrheumatologie gilt Cortison als Tiger-Medikament. Es ist stark wirksam und hilft sofort. Allerdings ist das Symbol des Tigers auch verbunden mit Gefährlichkeit, so dass es nicht ohne ärztliche Anleitung abgesetzt und gesteuert werden sollte.
Heutzutage werden Cortisonpräparate vorwiegend lokal angewandt, d. h. am Ort der Entzündung gegeben. Sehr gute Erfahrungen sind in den letzten 30 Jahren auch bei Kindern mit der Gelenkinjektion von Cortisonpräparaten gemacht worden, wenn eine qualifizierte und ausreichend lange Nachbehandlung der örtlichen Entzündung erfolgt. Hierdurch ist es möglich, auch stark bewegungseingeschränkte Gelenke mit Fehlstellungen wieder deutlich zu verbessern.
Örtliche Cortisontherapie
Im Vergleich zur Therapie mit nicht cortisonhaltigen Antirheumatika (NSAR) weist die örtliche Cortisoninjektion in die aktiv entzündeten Gelenke ein deutlich früheres und besseres Ansprechen sowie eine geringere Rate an Nebenwirkungen auf. Bei Verwendung eines Verzögerungspräparates mit längerer Verweildauer im Gelenk (Tramcinolon-Hexacetonid; Lederlon) ist die Wirkdauer Wochen bis Monate. Neben der hohen Wirksamkeit besteht eine gute Verträglichkeit. Schwere Nebenwirkungen wie Infektionen sind sehr selten, gelegentlich werden örtliche Veränderungen wie Rückgang des Unterhautfettgewebes oder Verkalkungen gesehen, die sich wieder zurückbilden können und keine funktionellen Auswirkungen haben. Eine anhaltende Störung des Hormongleichgewichts mit systemischen Zeichen der Cortisontherapie wird nach Injektionen kaum gesehen. Die Steuerungsfunktion der Hirnanhangdrüse kann jedoch für wenige Wochen verändert sein. Gelegentlich treten vorübergehend Veränderungen wie Appetitsteigerung, Gesichtsschwellung oder vermehrte Körperbehaarung auf. Die örtliche Injektionstherapie kann bei einem erneuten Auftreten der Entzündung wiederholt werden, der Ab- stand zwischen den Injektionen in das gleiche Gelenk sollte jedoch mindestens 3 Monate betragen.
Die Wirkung beginnt bereits nach einem Tag, erreicht ihr Maximum in den ersten 4 Wochen und kann abhängig von der Gelenkregion und Aktivität der Erkrankung länger als 1 Jahr anhalten. Eine Gelenkentlastung von mindestens 24 Stunden nach der Injektion wird empfohlen. Entscheidend ist jedoch die begleitende Behandlung mit Kälte- und Physiotherapie, bis eine vollständige Gelenkbeweglichkeit wieder hergestellt ist und entzündungsbedingte Fehlbelastungen sich zurückgebildet haben.
Durch eine frühzeitige örtliche Injektionsbehandlung in die entzündeten Gelenke können die Entzündung und mögliche Spätfolgen wie Bewegungseinschränkungen, Wachstumsstörungen, Muskelverkürzungen, Muskelatrophie, Achsenfehlstellungen und Kontrakturen verhindert oder zurückgebildet werden. Bei polyartikulären Verläufen kann durch frühzeitige Injektionsbehandlungen bereits eine weitgehende Rückbildung der örtlichen Entzündung erreicht sein, wenn die Wirkung des Basismedikamentes eintritt. Dies sind gute Voraussetzungen für ein Langzeit-Ansprechen („Remission“) unter diesem Therapieregime.
Auch für die örtliche Behandlung einer Regenbogenhautentzündung mit cortisonhaltigen Augentropfen sind diese Medikamente sehr wichtig. Ähnlich wie bei den Gelenkinjektionen kann auch der Augenarzt bei hoch aktiver Entzündung ein Cortisonpräparat in das Auge injizieren. Der Langzeitverlauf der entzündlichen Augenerkrankungen hat sich durch diese Präparate entscheidend bessern lassen.
Cortison als Infusionstherapie
Daneben ist Cortison gerade bei sehr schweren systemischen entzündlichen Erkrankungen als hoch dosierte Infusionstherapie in der Lage, den Verlauf der Erkrankung erheblich zu verbessern und Krankheitsschübe abzufangen oder zu verhindern. Die Therapie wird über 3 Tage als Infusion durchgeführt. Sie kann zunächst in etwa zweiwöchigen Abständen wiederholt werden. Die Intervalle werden bei gutem Ansprechen verlängert. Die Pulstherapie wird akut z. B. bei schwerer Herz- oder Augenbeteiligung sowie als überbrückende Maßnahme bis zur Wirksamkeit der übrigen Therapiemaßnahmen eingesetzt. Bei den Infusionsbehandlungen sollte eine gute klinische Überwachung erfolgen, da Kreislaufreaktionen möglich sind.
Nebenwirkungen von Cortison & Fazit
Die Häufigkeit und Schwere unerwünschter Wirkungen hängt im Wesentlichen von der Dauer der Cortison-Therapie und der Dosis ab. Hier sind neben dem typischen Aussehen mit Fetteinlagerung im Gesicht und am Stamm („Cushing-Syndrom“) eine vermehrte dunkle Körperbehaarung und Akne, diabetische Stoffwechsellage, eine gesteigerte Infektionsgefährdung, erhöhter Blutdruck, Muskelschwäche, Verhaltens- und Wesensveränderungen, Wachstumshemmung, Knochenentkalkung, ein erhöhtes Risiko für Magen-Darm-Geschwüre und Blutungen (insbesondere in Kombination mit NSAR), die Entstehung einer Thrombose, die Entwicklung einer Linsentrübung sowie eines erhöhten Augendruckes zu erwähnen.
Bei vielen Patient:innen lassen sich durch erfahrene Handhabung des Medikamentes entsprechend der bestehenden Entzündungsaktivität und der Risiken der rheumatischen Erkrankung diese Nebenwirkungen vermeiden oder reduzieren. Insbesondere ist es wesentlich, das Cortisonpräparat nach Möglichkeit nicht mehrfach täglich einzusetzen (am günstigsten ist eine Gabe morgens zwischen 6 und 8 Uhr), da sonst (durch Hemmung der Hormonsteuerung durch die Hirnanhangdrüse) ungünstige Einflüsse auf das Körperlängenwachstum zu erwarten sind.
Fazit:
Mit Cortisonpräparaten sind erfahrene Kinderrheumatolog:innen in der Lage, den Verlauf einer rheumatischen Entzündung mit chronischer Augen- oder Gelenkentzündung bzw. innerer Organbeteiligung entscheidend zu verbessern. Daher ist es wichtig, die Entscheidung zur Therapie mit Blick auf die Aktivität und die Risiken der Erkrankung gemeinsam zu treffen, die Dosis krankheitsangepasst frühzeitig zu minimieren und das Medikament, wenn möglich, nur zeitlich begrenzt einzusetzen.
Die Wirksamkeit und Verträglichkeit einer örtlichen Cortisonbehandlung ist ausgezeichnet. Diese Anwendung ist auch als Frühmaßnahme zur Behandlung einer Arthritis oder Uveitis geeignet. Auch bei einer vorübergehenden niedrig dosierten Cortisonbehandlung aufgrund hoher Entzündungsaktivität ist nicht mit Langzeitschäden durch das Medikament zu rechnen.
Eine frühzeitige, hochdosierte Behandlung im schweren Krankheitsschub (Pulstherapie) ist zur Kontrolle einer hohen Krankheitsaktivität geeignet und kann überbrückend eingesetzt werden. Ziel ist eine möglichst niedrig dosierte Dauertherapie mit Cortison unterhalb der Neben wirkungsschwelle bzw. die Beendigung nach Ansprechen auf die anderen Therapieformen.
Biologicals (Biologika)
Bei den Biologicals handelt sich um Eiweißpräparate, die aufgrund ihrer biologischen Eigenschaften direkt in den Entzündungsprozess eingreifen. Sie wirken spezifisch gegen bestimmte Entzündungsmechanismen im Körper.
Diese Medikamente haben unterschiedliche Angriffspunkte innerhalb der Zelle bzw. ihrer Mechanismen der Entzündungsabwehr. So können diese Substanzen wirksam sein z. B. durch den Einfluss auf entzündungsfördernde Eiweiße. Auch durch Veränderung der Erkennungsmechanismen an der Oberfläche der Entzündungszelle können Entzündungsvorgänge verhindert werden (z. B. bei Abatacept). Gentechnologisch hergestellte Eiweiße können so zum Beispiel einen speziellen Botenstoff der Entzündung blockieren, wie den sogenannten Tumor-Nekrose-Faktor TNF-alpha und hierdurch effektiv Entzündungsvorgänge unterdrücken.
Diese Medikamente haben die Behandlungsmöglichkeiten der rheumatischen Entzündungen entscheidend verbessert. Eine Vielzahl dieser neuen Präparate wird inzwischen auch bei Kindern und Jugendlichen eingesetzt.
Diese neueren Therapieansätze haben auch mögliche Risiken, die bedacht werden müssen. Hierzu gehört das Auftreten von Infektionen und selten das Entstehen von Störungen oder Krankheiten des Immunsystems. Vor Beginn einer Behandlung sollte eine sorgfältige kinderrheumatologische Risikoabwägung und Indikationsstellung erfolgen. Hierzu gehört auch, dass chronische Infektionen ausgeschlossen oder ausreichend behandelt sind. Bei allen Substanzen besteht ein gering erhöhtes Risiko, unter der Therapie an einer Tuberkulose zu erkranken. Daher ist der Ausschluss einer chronischen Infektion wie z. B. der Tuberkulose und der verschiedenen Formen der Hepatitis (Gelbsucht) vor Therapiebeginn erforderlich.
Es wird auch diskutiert, ob unter der Therapie ein erhöhtes Risiko für das Auftreten bösartiger Erkrankungen z. B. Lymphknotenkrebs besteht. Bisher gibt es diesbezüglich keine besorgniserregenden Daten. Diese Frage ist aber noch nicht abschließend für alle vorliegenden Substanzen zu beantworten. Daher sollte vor Beginn einer Therapie eine sorgfältige Prüfung der Indikation (Behandlungsgrundlage), der Begleitmedikamente und ihrer Risiken, der Ausschluss von Kontraindikationen (Hinderungsgründen) für die Behandlung sowie eine konsequente Überwachung der Patienten in einem kinderrheumatologischen Zentrum erfolgen. Die behandelten Patienten und Patientinnen können in einem Medikamentenregister erfasst werden, um die Wirksamkeit und das Auftreten seltener Nebenwirkungen zu registrieren. So können die Fragen der Langzeitnebenwirkungen dieser Präparate mit zunehmender Erfahrung und Langzeitanwendung besser beurteilt werden. Diese Medikamente werden bei Patient:innen eingesetzt, die eine schwere rheumatische Entzündung an zahlreichen Gelenken haben, auf eine konventionelle Therapie mit Gelenkinjektionen und Basistherapeutika unzureichend angesprochen haben oder aufgrund von Nebenwirkungen diese Therapien nicht mehr durchgeführt werden können.
Wirkprinzip von Etanercept
Wirkprinzip: Blockade von Tumor-Nekrose-Faktor TNF-alpha Etanercept
Etanercept ist ein Fusionsprotein (TNF-Rezeptor und Immunglobulin) und bindet an Tumor-Nekrose-Faktor TNF-alpha Die Wirksamkeit der Behandlung bei polyartikulärer JIA wurde in einer kontrollierten Studie nachgewiesen und die Substanz für die Behandlung dieser Indikation wurde ab 2 Jahren zugelassen, wenn die Erkrankung nicht auf MTX anspricht oder dieses aufgrund von Nebenwirkungen abgesetzt werden muss. Die Wirksamkeit und Langzeitverträglichkeit von Etanercept wurde in kleineren Studien nachgewiesen.
Etanercept wird in einer Dosis von 0,8mg/kg/Woche subcutan injiziert. Aufgrund der kurzen Halbwertszeit ist ein Injektionsintervall von 1– 2 x/Woche sinnvoll. Eine schlechtere Wirksamkeit konnte in einer kleineren Gruppe auch bei einer einmal wöchentlichen Injektion der o. g. Dosis nicht beobachtet werden.
Erfahrungen bestehen auch bei der Kombinationstherapie von Etanercept mit MTX im Kindesalter. Hierdurch erreichen mehr Patientinnen und Patienten einen vollständigen Rückgang der Entzündungsaktivität bei guter Verträglichkeit der Kombination. Die Anwendung dieser Substanzen kann durch Dokumentation in einem Arzneimittelregister der Gesellschaft für Kinder- und Jugendrheumatologie begleitet werden.
An Nebenwirkungen sind lokale Rötungen an der Einstichstelle häufig. Banale Nebenwirkungen wie Infektionen der oberen Luftwege, Kopfschmerzen, Bauchschmerzen, Erbrechen, Durchfallerkrankungen und Hautausschläge treten gelegentlich auf. Infektionen der Lunge, der Harnwege und anderer Lokalisationen bis zur eitrigen Infektion eines Gelenkes oder einer Sepsis wurden ebenfalls selten beobachtet.
An schweren nicht infektiösen Komplikationen werden unter anderem auch das Neuauftreten von Autoimmunerkrankungen (z. B. Morbus Crohn, Diabetes mellitus, Uveitis) sowie verschiedene onkologische Erkrankungen berichtet.
Wirkprinzip von Adalimumab
Adalimumab ist ein Eiweiß (ein humaner monoklonaler Antikörper), das gegen TNF-alpha gerichtet ist. Seine Wirksamkeit bei der polyartikulären JIA wurde in einer Studie gezeigt. Die Dosierung beträgt ab einem Alter von 2 Jahren 20 mg alle 2 Wochen bis zu einem Gewicht von 30 kg. Ab einem Gewicht von 30 kg 40 mg alle 2 Wochen. Das Medikament wird aufgrund seiner langen Halbwertszeit alle 2 Wochen subcutan injiziert. Im Vordergrund der Nebenwirkungen stehen auch hier Lokalreaktionen an der Einstichstelle.
Besonders zu erwähnen ist, dass diese Substanz auch gegen die therapieresistente Uveitis wirksam sein kann.
Das potentielle Nebenwirkungsspektrum ist bei den TNF-blockierenden Substanzen sehr ähnlich. Gelegentlich sieht man bei Adalimumab einen Wirkverlust durch Antikörper, die sich gegen das Medikament im eigenen Körper der Patienten bilden.
Es gibt noch weitere TNF-alpha-Hemmer wie Infliximab oder Golimumab, die ebenfalls zur Therapie von rheumatischen Erkrankungen bei Kindern und Jugendlichen eingesetzt werden.
Wirkprinzip von Anakinra
Wirkprinzip: Blockade von Interleukin 1
Interleukin 1 (IL 1) ist ein entzündungsförderndes Eiweiß, das von Zellen des Immunsystems und weißen Blutzellen (Monozyten, Makrophagen) gebildet wird. IL 1 stimuliert zahlreiche Mechanismen im Immunsystem, die die Entzündung unterstützen. Die Substanz kann gelegentlich auch für Symptome wie Fieber, Kopf- und Gliederschmerzen, Muskelschmerzen oder Appetitlosigkeit verantwortlich sein.
Anakinra ist ein Eiweiß, das gegen den IL-1-Rezeptor gerichtet ist. Es bindet an den Rezeptor und verhindert so ein stimulierendes Signal. Eine ausreichende Wirksamkeit bei polyartikulärer JIA konnte nicht gezeigt werden. Es besteht jedoch eine Zulassung für die Behandlung der systemischen JIA und anderer autoinflammatorischer Erkrankungen, die durch Anakinra sehr effektiv behandelt werden können. Das Medikament muss täglich injiziert werden. Im Vordergrund der Nebenwirkungen stehen örtliche Reaktionen an der Einstichstelle.
Als ein weiteres Medikament aus dieser Substanzgruppe mit längerer Halbwertszeit steht Canakinumab (IL-1ß-Antikörper) zur Verfügung, das ebenfalls für die systemische JIA und andere autoinflammatorische Erkrankungen zugelassen ist.
Wirkprinzip von Tocilizumab und Abatacept
Tocilizumab ist ein Eiweiß, das als Antikörper gegen den IL 6-Rezeptor zahlreiche Entzündungsvorgänge in Blutzellen, Leberzellen, Knochenzellen und im Gewebe hemmt. Die Aktivität von IL 6 wird durch den Antikörper neutralisiert.
Wirkprinzip Blockade von IL-6
Interleukin 6 ist ein zentrales Eiweiß, das bei vielen Entzündungsvorgängen des Körpers eine große Rolle spielt und bei Entzündungsvorgängen in vielen Geweben und Organen freigesetzt wird.
Die Wirksamkeit konnte sowohl bei der polyartrikulären als auch systemischen JIA in mehreren Studien gezeigt werden. Daher ist die Substanz zur Behandlung der systemischen und polyartikulären JIA zugelassen.
Abatacept
In einer kontrollierten Studie konnte die Wirksamkeit von Abatacept bei der polyartikulären therapierefraktären JIA nachgewiesen werden. Ein therapeutischer Effekt ist erst nach mehrmonatiger Behandlung zu erwarten.
Wirkprinzip: Blockade der Ko-Stimulation von T-Lymphozyten
Damit eine Stimulation von T-Zellen erfolgt, müssen zwei Signale die Zelle erreichen. Ein künstlich hergestelltes Eiweiß (Abatacept) bindet an der Zelloberfläche der Entzündungszelle und verhindert so eine Aktivierung der T-Zelle. Hierdurch werden bestimmte Reaktionen im Ablauf einer Entzündung nicht ausgelöst.
Die Substanz ist ab 6 Jahren zugelassen zur Behandlung der mäßigen bis schweren polyartikulären JIA (in Kombination mit MTX), wenn das Ansprechen auf TNF-Antagonisten (und andere Basistherapeutika) nicht ausreichend ist.
Wirkprinzip von Tofacitinib, Baricitinib und Upadacitinib
Tofacitinib, Baricitinib und Upadacitinib sind Januskinase-Hemmer (JAK-Hemmer) und für die Behandlung von kindlichen Autoimmunerkrankungen geeignet. Diese neuen Medikamente greifen gezielt in das Immunsystem ein, indem sie Januskinasen (JAK) hemmen, die für die Signalübertragung entzündungsfördernder Botenstoffe verantwortlich sind. Sie wirken in der Zelle und werden auch als kleine Moleküle („small molecules“) bezeichnet. Sie werden als Tabletten oder bei kleinen Kindern als Lösung eingenommen und wirken, indem sie die Signalwege in den Immunzellen blockieren, was zur Unterbrechung des Krankheitsprozesses führt. Ihr Einsatz erfolgt insbesondere bei juveniler idiopathischer Arthritis (JIA), wenn andere Therapien nicht ausreichen. Aktuell werden diese Substanzen auch für die Behandlung der systemischen JIA überprüft. Tofacitinib und Baricitinib sind bereits ab dem Alter von 2 Jahren für bestimmte JIA-Kategorien zugelassen.
Fazit zum Einsatz von Biologika und JAK-Hemmern
Die Weiterentwicklung der Biologika und JAK-Inhibitoren lässt für die Behandlung der JIA hoffen, dass das Therapieziel „Remission“ durch Kombination von Behandlungsmethoden für möglichst alle JIA-Patienten erreichbar ist.
Die Langzeitrisiken der neuen Substanzen sind noch nicht abschließend beurteilbar. Daher ist die Erfassung dieser Medikamente in Therapieregistern wichtig für die Beurteilung der Wirksamkeit und der Arzneimittelsicherheit.
Daher sollten diese Medikamente derzeit nur durch kinderrheumatologisch erfahrene Ärzte unter regelmäßiger Kontrolle eingesetzt werden.
FAQ zu Kinderrheuma-Medikamenten
Was können die Medikamente insgesamt erreichen?
Die Medikamente können die Folgen der Entzündung, d. h. die Schwellung, vermehrte Durchblutung und Funktionseinschränkungen zurückbilden und so dabei helfen, Dauerschäden an den Gelenken zu vermeiden. Sowohl die Bildung von Entzündungseiweißen, als auch die Vermehrung von Entzündungszellen im Gelenk, im Blut sowie in den Organen des Abwehrsystems werden reduziert. Hierdurch wird die Aktivität der Entzündung insgesamt herabgesetzt. Verschiedene Medikamente haben unterschiedliche Angriffspunkte innerhalb dieses Wirksystems und können sich gegenseitig ergänzen. Insbesondere eine Kombination aus nichtcortisonhaltigen Antirheumatika, örtlicher Cortisonbehandlung und langwirksamen Antirheumatika wird aufgrund der unterschiedlichen Wirkweisen und Angriffspunkte als effizient angesehen.
Welches sind die Ziele der medikamentösen Therapie bei rheumatischen Erkrankungen?
Prinzipiell haben die Medikamente das Ziel, eine möglichst schnelle Kontrolle der Entzündung herbeizuführen, um Langzeitschäden zu vermeiden. Diese Entzündungskontrolle ist Voraussetzung für den Rückgang der Schwellung, des Schmerzes und der Fehlbelastung und somit auch wesentliche Voraussetzung für die Effektivität physikalischer Therapiemaßnahmen, wie z. B. der Krankengymnastik. Durch die Kontrolle der Entzündung kann es zu einer Wiederherstellung der natürlichen Gelenkfunktionen kommen. Im Stadium der akuten Entzündung entsteht auch ein Ungleichgewicht der muskulären Belastung mit Verkürzung der Beugemuskulatur und Abnahme der Streckmuskulatur. Die Verkürzung der Beugemuskulatur mit Beugefehlstellung des Gelenks nennt man Kontraktur.
Diese Komplikation ist oft Ursache für eine langwierige und intensive Krankenhausbehandlung, so dass ein wesentliches Ziel darin besteht, entzündungsbedingte Gelenkkontrakturen zu verhindern. Ferner haben die Medikamente das Ziel, Langzeitschäden an inneren Organen zu vermeiden, die z. B. durch überschüssige Produktion von Entzündungseiweißen entstehen können.
Welches sind die Kriterien für eine effektive medikamentöse Behandlung?
Im Wesentlichen wird der Entzündungsverlauf anhand der Gelenkbeweglichkeit beurteilt. Eine medikamentöse Behandlung ist dann effektiv, wenn durch Rückgang der Schwellung, Überwärmung und Bewegungseinschränkung eine freie Beweglichkeit der Gelenke wieder möglich wird. Auch die Bildgebung wie Ultraschall oder MRT kann den Rückgang der Entzündungsaktivität nachweisen und dokumentieren.
Darüber hinaus wird die Effektivität der medikamentösen Behandlung auch an den Entzündungswerten im Blut gemessen. Hierzu gehören der Rückgang einer erhöhten Blutsenkungsgeschwindigkeit, der Entzündungseiweiße (z. B. des CRP), der Rückgang einer Anämie (Verminderung der roten Blutkörperchen) und einer erhöhten Leukozytenzahl (weiße Blutkörperchen).
Anhand des Krankheitsverlaufs wird über Beibehaltung, Erweiterung oder Rücknahme der medikamentösen Therapie entschieden. Die Zeitdauer der medikamentösen Behandlung ist zu Behandlungsbeginn noch nicht beurteilbar.
Ist der Behandlungsverlauf vorhersehbar?
Bei verschiedenen rheumatischen Erkrankungen mit Manifestation an Gelenken oder inneren Organen können im Einzelfall Wochen bis Monate vergehen, bis die Effektivität der Behandlung erkennbar oder abschätzbar wird. Hinzu kommt, dass für jedes einzelne Kind die Wirksamkeit eines Medikaments nicht sicher vorhersehbar ist. Beispielsweise kann sich während der Behandlung der Erkrankung die Stärke der Entzündung ändern.
Medikamente werden in Abhängigkeit vom Krankheitsstadium oder der Krankheitssituation unterschiedlich vom Körper aufgenommen oder verarbeitet. Die Effektivität der Behandlung muss im Einzelfall immer wieder neu beurteilt werden. Hierzu dienen die regelmäßigen Verlaufskontrollen.
Es bestehen bei der Behandlung rheumakranker Kinder und Jugendlicher somit allgemeine Therapieprinzipien, jedoch keine feststehenden Behandlungsprotokolle, die die Therapie über Monate und Jahre steuern. Dies liegt an der großen Variation der Erkrankungsverläufe und der Notwendigkeit einer individuellen Behandlungsanpassung. Ein möglicher Nachteil fehlender Schemata liegt darin, dass die Behandlung sich in hohem Maße an der Erfahrung der behandelnden Ärzt:innen orientiert.
Vergleichbarkeit und Effektivität der Behandlung ist daher nur eingeschränkt möglich. Wichtig für den Behandlungserfolg ist die engmaschige, langjährige Kooperation zwischen Patient, Eltern und behandelnden Ärzten, da Therapieentscheidungen bei genauer Kenntnis des Verlaufs leichter sind.
In vielen Fällen ist eine wirksame medikamentöse Behandlung möglich. Bei konsequenter und rasch einsetzender Behandlung können die Langzeitprobleme der Erkrankung verringert werden.
Kann man die Nebenwirkungen einer medikamentösen Therapie über Monate und Jahre in Kauf nehmen?
Neben den erwünschten Wirkungen der Medikamente besitzt jedes Medikament auch Nebenwirkungen. Leichte Nebenwirkungen sind Unverträglichkeiten, die das Kind nicht gefährden. Hierunter versteht man z. B. Störungen wie Übelkeit oder Appetitlosigkeit. Alle Medikamente können prinzipiell auch zu allergischen Reaktionen führen und müssen dann im Langzeitverlauf abgesetzt werden.
Ernsthafte Nebenwirkungen sind in erster Linie solche, die lebenswichtige Organe betreffen, insbesondere wenn sie unbemerkt ablaufen. Wir unterscheiden häufige, rückbildungsfähige und seltene nichtrückbildungsfähige Nebenwirkungen.
Nebenwirkungen sind oft dosisabhängig. Nach dem Erkennen des Problems und der Verminderung der Medikamentenmenge oder dem Absetzen des Medikaments bilden sich die Nebenwirkungen in der Regel zurück. Ein Beispiel ist der Anstieg der Leberwerte unter Methotrexat oder die Übelkeit unter diesem Medikament.
Die Packungsinformation des Herstellers enthält die bisher beobachteten Nebenwirkungen eines Medikaments. Hier werden seltene oder häufige Nebenwirkungen gleichzeitig genannt. Viele Nebenwirkungen sind durch regelmäßige Kontrollen und entsprechende Informationen der Patienten und Eltern gut einzuschätzen.
Im Grunde gilt unabhängig von Erkrankung und Verlauf: Vor jeder Entscheidung zu einer medikamentösen Behandlung müssen die Risiken der Erkrankung und ihre möglichen Folgen das Nebenwirkungsrisiko der medikamentösen Therapie deutlich überwiegen. Zur Minimierung des Risikos sind regelmäßige Untersuchungen sowie Blut- und Urinkontrollen sinnvoll.
Welchen Sinn haben die Packungsinformationen der Medikamente?
In den Packungsinformationen wird die sogenannte Darreichungsform des Medikaments erwähnt, d. h. ob die Substanz als Saft, Zäpfchen, Tablette, Dragee oder Injektion zur Verfügung steht und in welcher Konzentration der Wirkstoff enthalten ist.
Auch die üblichen Dosierungen sind angegeben. Diese können jedoch von der ärztlichen Empfehlung abweichen. Falls das Medikament nach Anbruch der Packung eine bestimmte Haltbarkeit besitzt, ist diese auch in der Packungsinformation enthalten, ansonsten ist auf den Medikamentenpackungen „verwendbar bis...“ mit Datum angegeben.
Der Hersteller informiert über alle bislang beobachteten Nebenwirkungen sowie über die ihres jeweiligen Auftretens.
Warum ist eine Langzeittherapie sinnvoll und erforderlich? Bei rheumatischen Erkrankungen im Kindes- und Jugendalter zeigt die Erfahrung, dass eine kurzzeitige Therapie für die chronische Entzündung nicht effektiv ist. Ein unmittelbares Absetzen der Medikamente nach Besserung und Ausheilung der akuten Entzündung ist nicht sinnvoll, da die Gefahr eines Rückfalls besteht, der auch über Monate schleichend auftreten kann. Unauffällige körperliche Untersuchungsbefunde und Laboruntersuchungen sind kein Beweis für eine Ausheilung einer rheumatischen Erkrankung, d. h. auch wenn keine Entzündung mit unseren heutigen Untersuchungsmöglichkeiten nachweisbar ist, können ruhende Entzündungszellen die Erkrankung später wieder aktiv werden lassen.
Die medikamentöse Behandlung ist aus diesen Gründen oft über mehrere Jahre erforderlich und muss in jedem Einzelfall individuell beurteilt werden.
Kann man auch Medikamente miteinander kombinieren?
Der gleichzeitige Einsatz mehrerer Medikamente kann vielfach sinnvoll sein, da sich diese in ihrer Wirksamkeit gegenüber der Entzündung ergänzen. Es werden in der Regel Medikamentenkombinationen gewählt, deren unterschiedlicher Wirkmechanismus und Angriffspunkt keine deutlich erhöhten Nebenwirkungsrisiken mit sich bringen. Nicht sinnvolle Medikamentenkombinationen sind z. B. mehrere nichtcortisonhaltige Antirheumatika, da es vorwiegend zu einem erhöhten Nebenwirkungsrisiko, z. B. für den Magen- Darmtrakt, kommen kann, ohne dass die Wirkung wesentlich verstärkt wird. Auch die Kombination mehrerer cortisonähnlicher Präparate bedeutet keine bessere Effektivität. Dies gilt jedoch nicht für die zusätzliche örtliche Cortisonbehandlung, z. B. durch Gelenkinjektion oder cortisonhaltige Augentropfen.
Andererseits kann eine Kombination von Cortison mit Immunsuppressiva sinnvoll sein, um die Cortisondosis in der Langzeitbehandlung möglichst niedrig zu halten und die Wirkmechanismen der Basistherapie zu unterstützen. So zeigt eine Studie bei Rheumatikern im Erwachsenenalter ein deutlich langsameres Fortschreiten der knöchernen Veränderungen bei Kombinationsbehandlung von Methotrexat und niedrigdosiertem Cortison. In Einzelfällen können sich jedoch die Nebenwirkungen auch bei rheumatologisch sinnvollen Medikamentenkombinationen verstärken, daher sollten Veränderungen der körperlichen Befindlichkeit beobachtet und dem behandelnden Arzt rasch mitgeteilt werden. Insbesondere Änderungen der Körperausscheidung,
z. B. Erbrechen von bluthaltiger Flüssigkeit oder Absetzen von sehr dunklem Stuhl, sollten unmittelbar mit dem Behandler besprochen werden. Bei diesen Symptomen sollten die Medikamente bereits bei Verdacht auf eine Nebenwirkung abgesetzt werden.
Eine Kombination von Methotrexat und Biologika wird sehr häufig angewendet, da sich beide Substanzen gut ergänzen können. Eine Kombination von unterschiedlichen Biologika oder JAK-Hemmern ist aktuell noch eine „off-label“-Ausnahme (außerhalb der üblichen Zulassung) und darf nur in Einzelfällen unter strenger Überwachung und Indikation durch einen erfahrenen Kinderrheumatologen erfolgen.
Welche Dosierungen und Darreichungen sind für Kinder sinnvoll?
Die meisten Medikamente besitzen einen festgelegten Behandlungsbereich, d. h. eine empfohlene Dosierung, bei der von einer Wirksamkeit bei relativ geringem Nebenwirkungsrisiko auszugehen ist. Dosisunterschreitungen können zur Ineffektivität der Behandlung führen. Dosisüberschreitungen haben oft keinen zusätzlichen Behandlungseffekt, jedoch ein erhöhtes Nebenwirkungsrisiko.
In der Langzeittherapie können auch sehr niedrige Dosierungen noch entzündungshemmende Effekte besitzen, speziell gilt dies für eine niedrig dosierte Cortisontherapie.
Jedes Medikament wird aufgrund seiner biologischen Daten für Aufnahme, Verarbeitung und Ausscheidung im Körper dosiert. Medikamente mit einer kurzen Halbwertszeit müssen mehrfach täglich gegeben werden, da sie innerhalb weniger Stunden bereits zum größten Teil aus dem Körper ausgeschieden werden.
Aufgrund der Daten des Medikamentenherstellers zur Halbwertszeit und der bio- logischen Wirksamkeit ergibt sich die Empfehlung, ein Medikament auf eine oder mehrere Gaben pro Tag zu verteilen. Die meisten Substanzen werden als Tablette, Dragee oder Saft gegeben.
Bei einigen Medikamenten ist eine Wirkungsverstärkung durch die Gabe des Medikaments in die Blutbahnen intravenös (i. v.), in die Muskulatur (i. m.) oder unter die Haut (subcutan) im Vergleich zur Tablettenapplikation5 gegeben. Dies gilt ins- besondere für Methotrexat, wo Dosis und Applikationsform im Einzelfall miteinander besprochen werden sollten. Die Injektionen unter die Haut (s. c.) können von den Eltern und Patienten für die regelmäßige Anwendung zu Hause erlernt wer- den.
Einige der in der Kinder- und Jugendrheumatologie verwendeten Medikamente sind nicht speziell für das Kindes- und Jugendalter zu- gelassen. Der Einsatz beruht jedoch oft auf jahrzehntelanger Erfahrung bei rheumatischen Entzündungen bei Kindern und Jugendlichen. Vor dem Einsatz eines Medikaments werden Familie und Patient ausführlich über Wirkweise, Dosierung, Darreichungsformen und Therapieziele informiert. Patienten und Eltern sollten die Produktinformation zur Kenntnis nehmen und sich nicht scheuen, ihre Fragen mit den Ärzt:innen offen anzusprechen, damit eine Langzeitakzeptanz des Medikaments möglich ist.
Wichtig ist, Dosis und tageszeitliche Verteilung regelmäßig zu beachten. Auch die Medikamentenform als Tablette, Saft oder Ampulle sollte besprochen und nur nach ärztlicher Rücksprache geändert werden.
Was ist zu beachten, wenn zusätzliche Medikamente bei akuten Erkrankungen erforderlich sind?
Bei akuten Erkrankungen können zusätzlich andere Medikamente erforderlich werden, z. B. Antibiotika bei Infektionskrankheiten. Es ist sehr wichtig, dass plötzlich auftretendes Fieber noch am gleichen Tag ärztlich abgeklärt und evtl. behandelt wird. Wenn Medikamente zusätzlich ärztlich verordnet werden, also auch beim ärztlichen Notdienst am Wochenende, sollte die aktuelle Behandlung des Rheumas immer mitberücksichtigt werden. Die Verordnung sollte jedoch nicht dazu führen, dass bei bestehender Indikation, z. B. einer eitrigen Infektionen im Körper, nicht ausreichend z. B. mit Antibiotika behandelt wird, da die Infektion eine zusätzliche Gefahr darstellen und einen neuen Rheumaschub auslösen kann.
Wie kann eine vertrauensvolle Zusammenarbeit zwischen Patient:in/Eltern und behandelnden Ärzt:innen aufgebaut werden?
Die Frage nach Verträglichkeit und Wirksamkeit von Medikamenten spielt für Eltern/Kinder und die betreuenden Ärzt:innen eine bedeutende Rolle. Entscheidend ist, die Probleme des Kindes und der Eltern stets gezielt anzusprechen, um sinnvolle Möglichkeiten der Weiterbehandlung planen zu können und Risiken der Selbsttherapie zu minimieren. Eine vertrauensvolle Therapievereinbarung zwischen Patient:in/Ärzt:in und Eltern ist wichtig für eine sinnvolle Steuerung der medikamentösen Behandlung. Dies gilt auch für zusätzlich angesetzte Medikamente, wie z. B. pflanzliche Präparate, oder eine homöopathische Behandlung. Oft haben die mit der Rheumabehandlung befassten Ärzt:innen auch Erfahrungen mit sogenannten Alternativtherapien, das Thema wird aber aus falscher Scheu von den Eltern oft nicht angesprochen.
Zusätzliche Therapien können häufig durchaus toleriert werden, wenn sie nicht zu einer Stimulation des Immunsystems und somit auch der rheumatischen Entzündung führen. In jedem Falle sollten zusätzliche Therapien im Gespräch Erwähnung finden. Wenn Medikamente nicht eingenommen oder abgesetzt werden, muss der Arzt oder die Ärztin dies frühzeitig erfahren. Ebenso ist die Begründung, warum dies erfolgte, sehr wichtig. Informationsdefizite können zu einer ärztlichen Fehlbeurteilung führen.
Kinderrheuma & Therapie
In diesem Kurzinterview beantwortet PD Dr. Daniel Windschall, Chefarzt der Klinik für Kinder- und Jugendrheumatologie im St. Josef-Stift Sendenhorst, Fragen rund um das Thema Kinderrheuma und Therapie. Dieses Video ist Teil der Schulungsfilmreihe über Kinder- und Jugendrheuma vom Bundesverband Kinderrheuma e. V. und zeigt die Arbeit der Klinik für Kinder- und Jugendrheumatologie im St. Josef-Stift Sendenhorst. Die Schulungsfilme behandeln die Themen Diagnostik, Therapie, Physiotherapie, Ergotherapie, Schule, Soziales, Krankheitsbewältigung und Selbsthilfe.
Ambulante Kontrolle & ASV Kinderrheumatologie
Kinder mit rheumatischen Erkrankungen benötigen neben der stationären Behandlung auch eine regelmäßige und gut abgestimmte ambulante Betreuung. Auch in den Phasen der Entzündungsfreiheit ist eine kinderrheumatologische Betreuung und Kontrolle in bestimmten Abständen wichtig.
Ziel ist es, die Entzündung in den Gelenken immer frühzeitig zu behandeln, Krankheitsschübe zu erkennen und eine gesunde körperliche und soziale Entwicklung zu ermöglichen.
Stationär und ambulant - Hand in Hand
Optimalerweise entsteht zwischen stationärer und ambulanter Behandlung eine umfassende und gut abgestimmte Betreuung.
Die kinder- oder hausärztliche Betreuung spielt eine wichtige Rolle, indem sie die allgemeine Betreuung vor Ort übernimmt und zum Beispiel auf Impfungen achtet. Da bei manchen Kindern zusätzlich eine Augenentzündung auftreten kann, gehören auch regelmäßige augenärztliche Untersuchungen dazu. Ebenso sind Physiotherapie und Ergotherapie an der ambulanten Versorgung beteiligt, die durch Übungen und Training helfen, Beweglichkeit und Muskelkraft zu erhalten und den Alltag besser zu bewältigen.
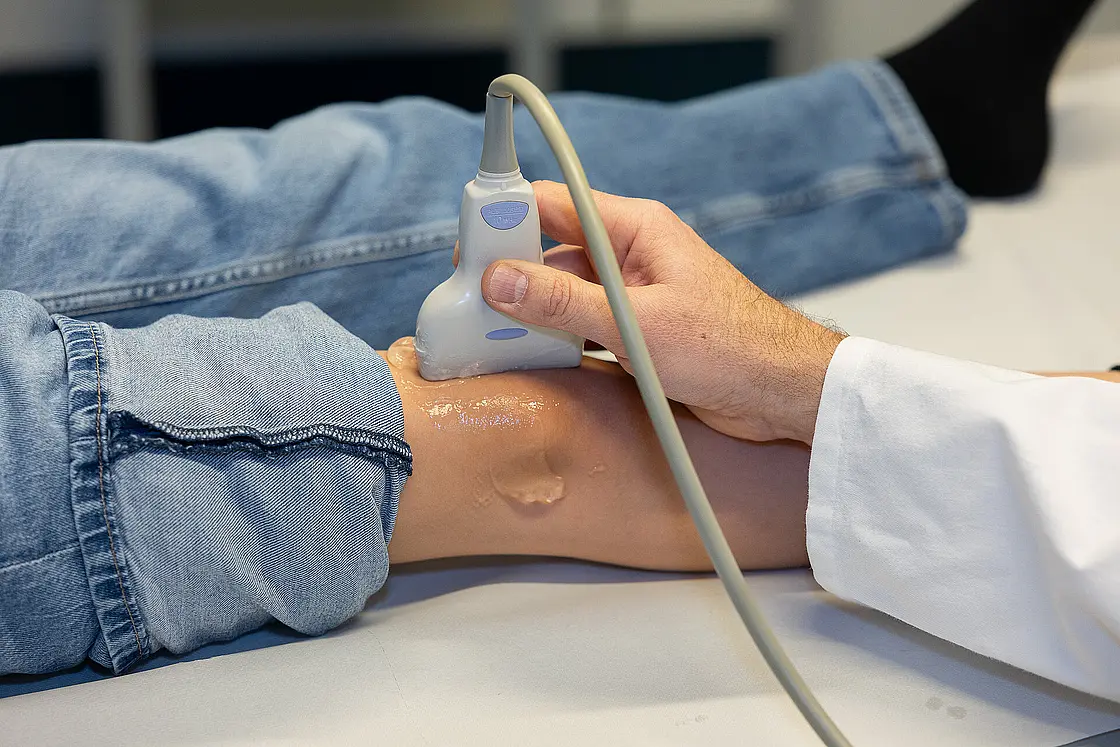
Bei den regelmäßigen Kontrollen werden Blutuntersuchungen durchgeführt, um Entzündungswerte und mögliche Nebenwirkungen der Medikamente zu überwachen. Zusätzlich können bildgebende Verfahren wie Gelenk-Ultraschall eingesetzt werden. Mit der körperlichen Untersuchung können Wachstum, Beweglichkeit und allgemeines Wohlbefinden beurteilt werden. Gespräche über Schmerzen, Schule und Freizeit sind ebenfalls Teil der Betreuung, damit die Behandlung gut in den Alltag passt.
Die Klinik für Kinder- und Jugendrheumatologie versorgt Kinder und Jugendliche bis zum 21. Lebensjahr in einer Ermächtigungsambulanz und zusätzlich in einer ASV-Sprechstunde.
ASV Kinderrheumatologie
Ein besonderer Baustein in der ambulanten Versorgung ist die sogenannte ASV-Ambulanz, die für „Ambulante Spezialfachärztliche Versorgung“ steht. Dort arbeiten im Rahmen der ASV „Kinderrheumatologie“ verschiedene Fachärzt:innen aus den Bereichen Kinderrheumatologie, Augenheilkunde, Orthopädie, Radiologie, Labormedizin, Dermatologie und weitere Fachbereiche eng zusammen. Alles ist unter einem Dach eng vernetzt, so dass die verschiedenen Fachrichtungen die Behandlung auf kurzem Wege gut miteinander abstimmen können. Gerade für Kinder mit einem komplexeren Verlauf oder seltenen Formen der Erkrankung ist das ein großer Vorteil. Die Kosten werden von der Krankenkasse übernommen. Für die ASV ist eine besondere Überweisung §116b SGB V notwendig.